
Definiție
– Expectorație de sânge din tractul respirator inferior
– Simptom rar, dar grav la pacienții pediatrici
– Poate varia de la episoade ușoare, care se remit de la sine, până la hemoragii pulmonare care pun viața în pericol și necesită intervenție urgentă.
– Mult mai puțin frecvent decât la adulți
– adesea un indiciu al unei afecțiuni grave subiacente, inclusiv infecții, anomalii congenitale, malformații vasculare sau boli autoimune
Hemoptizia în reumatologia pediatrică
Hemoptizie acută vs. cronică
Hemoptizie acută
– Apare brusc, durează de obicei câteva ore până la câteva zile
– Adesea asociată cu inflamație acută sau cu o exacerbare bruscă a unei boli subiacente
– Mai probabilă să fie severă și să progreseze rapid la copii, în special în sindroamele pulmonar-renale
– Cauze
o Hemoragie alveolară difuză (DAH): O manifestare severă a lupusului eritematos sistemic (LES), vasculitei asociate cu ANCA (AAV) și sindromului Goodpasture (GPS)
o Vasculită IgA (denumită anterior purpură Henoch Schönlein): cauză extrem de rară de hemoragie pulmonară, dar poate fi asociată cu afectare renală severă
o Exacerbări acute ale vasculitei asociate cu ANCA (AAV) sau pneumonitei lupice.
Hemoptizie cronică
– Spută persistentă sau recurentă cu sânge pe o perioadă de săptămâni sau luni
– Mai probabilă din cauza unei boli pulmonare inflamatorii cronice, a unei hemoragii alveolare recurente sau a unei tulburări genetice
– Pacienții pediatrici nu raportează întotdeauna hemoptizia ușoară, ceea ce întârzie diagnosticul
– Cauze:
o Sindromul COPA: o afecțiune autoimună monogenică care se manifestă prin hemoragie alveolară recurentă și boală pulmonară interstițială la copii.
o Hemosideroză pulmonară idiopatică (IPH): O cauză cronică a sângerării alveolare recurente, care duce la depunerea de fier, anemie și fibroză pulmonară
o Hemoragie alveolară recurentă asociată cu vasculită, în special în cazul AAV recidivant.
Hemosideroza pulmonară idiopatică (IPH)
– O afecțiune pediatrică rară caracterizată prin hemoragie alveolară difuză recurentă
– Etiologia rămâne necunoscută, dar unele cazuri sunt asociate cu procese autoimune
– Triada clinică: hemoptizie recurentă, anemie feriprivă, infiltrate pulmonare difuze
– Diagnostic:
o CT de înaltă rezoluție (HRCT): prezintă opacități difuze în sticlă mată și depuneri de hemosiderină
o Lavaj bronhoalveolar (BAL): prezența macrofagelor încărcate cu hemosiderină
o Biopsie pulmonară: utilă în cazurile atipice
– Tratament
o Prima linie: corticosteroizi pentru reducerea inflamației
o Imunosupresoare: Rituximab sau azatioprină în cazurile refractare
o Tratament de susținere
Sindromul COPA
– O afecțiune autoimună monogenică cauzată de mutații ale genei COPA (autozomal dominantă)
– Prezentare clinică: hemoragie alveolară recurentă, boală pulmonară interstițială, artrită și afectare renală
– Apare frecvent la copii, simptomele manifestându-se încă din perioada sugarului
– Diagnostic
o Testare genetică pentru mutații COPA.
o HRCT: prezintă boală pulmonară interstițială și opacități în sticlă mată
o BAL: macrofage încărcate cu hemosiderină
– Tratament
o Prima linie: Corticosteroizi pentru reducerea inflamației
o Imunosupresoare (rituximab, ciclofosfamidă)
o Agenți biologici care vizează IL-6 sau TNF-α
Vasculită IgA (vezi capitolul separat)
– Cea mai frecventă vasculită pediatrică, dar rareori provoacă hemoragie pulmonară
Lupus eritematos sistemic și hemoragie alveolară difuză (vezi capitolul separat)
– SLE pediatric se manifestă adesea cu afectarea mai severă a organelor decât SLE cu debut la adulți.
– Hemoragia alveolară difuză (DAH) este rară, dar pune viața în pericol.
– Factori de risc:
o Activitate ridicată a bolii (scor SLEDAI).
o Nefrita lupică.
o Prezența anticorpilor antifosfolipidici.
– Diagnosticul SLE:
o ANA (titru ≥1:80) – necesar
o Criterii clinice (constituționale, hematologice, neuropsihiatrice, mucocutanate, seroase, musculo-scheletale, renale)
o Criterii imunologice
– Diagnosticul DAH:
o HRCT: Opacități difuze în sticlă mată și consolidare alveolară.
o BAL: lichid hemoragic cu macrofage încărcate cu hemosiderină
– Tratament
o Corticosteroizi în doze mari
o Ciclofosfamidă sau rituximab
o Plasmafereză în cazuri severe
Vasculită asociată cu ANCA la copii (vezi capitolul separat)
– Include granulomatoza cu poliangeită (GPA), poliangeita microscopică (MPA) și granulomatoza eozinofilică cu poliangeită (EGPA)
– AAV pediatrică este agresivă, prezentându-se adesea cu glomerulonefrită rapid progresivă (RPGN) și hemoragie alveolară
– Diagnostic:
o Serologie ANCA (anticorpi PR3/MPO).
o Biopsie renală: Prezintă glomerulonefrită necrozantă pauci-imună
o Biopsie pulmonară, dacă este necesar
– Tratament
o Terapie de inducție: corticosteroizi + ciclofosfamidă sau rituximab.
o Întreținere: Azatioprină, micofenolat mofetil (MMF) sau rituximab
o Plasmafereză în cazuri severe
Sindromul Goodpasture (GPS) la copii
– Extrem de rar în pediatrie.
– Cauzat de anticorpi anti-membrană bazală glomerulară (GBM), care duc la hemoragie alveolară și glomerulonefrită rapid progresivă
– Diagnostic:
o Testarea anticorpilor anti-GBM.
o Biopsie renală
– Tratament
o Plasmafereză
o Corticosteroizi + ciclofosfamidă.
Concluzie
– Hemoptizia pediatrică cauzată de boli autoimune este rară, dar poate pune viața în pericol
– Trebuie excluse cauzele mai frecvente ale hemoptiziei
– Sindroamele pulmonar-renale (AAV, GPS, COPA, SLE) trebuie recunoscute prompt și tratate agresiv
– Diagnosticul precoce și terapia imunosupresivă sunt cruciale pentru îmbunătățirea rezultatelor.
– Direcțiile viitoare includ terapii biologice țintite și screening genetic pentru cauze monogenice, cum ar fi sindromul COPA
Diagnosticul diferențial al hemoptiziei la copii:
– Cauze infecțioase
o Pneumonie bacteriană (de exemplu, Staphylococcus aureus, Streptococcus pneumoniae, Klebsiella)
o Tuberculoză (TB) – TB primară sau reactivată
o Infecții fungice (de exemplu, aspergiloză, histoplasmoză, mucormicoză)
o Pneumonie virală (de exemplu, gripă, RSV, adenovirus)
o Infecții parazitare (de exemplu, hidatidoză, paragonimoză în zone endemice)
– Cauze autoimune și vasculitice
o Vasculită sistemică primară
▪ Vasculită asociată cu ANCA (granulomatoză cu poliangeită, poliangeită microscopică)
▪ Vasculită IgA – Afectare pulmonară rară
o Lupus eritematos sistemic (LES) – Hemoragie alveolară difuză, pneumonită lupică
o Sindromul Goodpasture (boala anti-GBM) – Hemoragie pulmonară și glomerulonefrită
o Hemosideroză pulmonară idiopatică (IPH) – Hemoragie alveolară recurentă fără boală sistemică
o Sindromul COPA – Tulburare monogenică cu hemoragie alveolară, artrită și boală renală
– Cauze cardiovasculare
o Boli cardiace congenitale, malformații arteriovenoase pulmonare (AVM) – telangiectazie hemoragică ereditară (HHT), hipertensiune pulmonară
– Anomalii ale căilor respiratorii și structurale
o Aspirație de corp străin, bronșiectazie, malformații traheobronșice, neoplasm (rar)
– Traume și cauze iatrogene
– Tulburări hematologice și de coagulare
o Trombocitopenie, hemofilie, coagulopatie (de exemplu, sindroame de coagulare intravasculară diseminată)
– Cauze de mediu și toxice
Hemoragie alveolară difuză datorată vasculitei
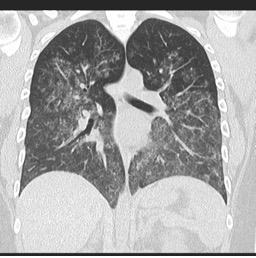
Sursa: radiopaedia.org
Text pregătit de Nikol Husáková (nikol.husakova@vfn.cz), pe baza următoarelor resurse:
- Laya BF, Concepcion NF. Hemoptysis in children: Imaging evaluation. Pediatr Radiol. 2007;37(12):1211–1223. doi:10.1007/s00247-007-0609-6
- Weiss PF. Pediatric vasculitis. Pediatr Clin North Am. 2012;59(2):407–423. doi:10.1016/j.pcl.2012.03.005
- Kitching AR, Anders HJ, Basu N, Brouwer E, Gordon J, Jayne DR, et al. ANCA-associated vasculitis. Nat Rev Dis Primers. 2020;6(1):71. doi:10.1038/s41572-020-0204-y
- Tanaka C, Benseler SM. Systemic lupus erythematosus in children and adolescents. Pediatr Clin North Am. 2017;64(2):339–361. doi:10.1016/j.pcl.2016.11.008
- Green RJ, Ruoss SJ, Kraft SA, Berry GJ, Raffin TA. Idiopathic pulmonary hemosiderosis in children: Diagnostic criteria, management, and outcome. Eur Respir J. 2001;17(3):496–501. doi:10.1183/09031936.01.17304960
- Griese M, Kabra SK, Tan HL. Pulmonary hemorrhage in children: Diagnostic workup and therapeutic approaches. Paediatr Respir Rev. 2011;12(3):231–238. doi:10.1016/j.prrv.2011.03.005








